尋媶撪梕
摉嫵幒偱偼丄埲壓偺尋媶傪峴偭偰偄傑偡丅
- 検巕價乕儉媄弍PIXE/PIGE偵傛傞乽嶍傜側偄乿偆怚帯椕偺幚尰
- 僶僀僆儈僱儔儕僛乕僔儑儞丒儊僇僯僘儉偵婎偯偔崅楊幰偺偆怚梊杊丒帯椕朄偺奐敪
- 幐妶帟偺岠壥揑側曗嫮曽朄偺扵嶕
- 僨乕僞儅僀僯儞僌庤朄傪梡偄偨僇儕僄僗儕僗僋梊應
- 柶塽丒崪戙幱偺晩妶壔偵傛傞帯桙懀恑傪慱偭偨師悽戙崻娗揬栻嵻偺奐敪
- 徾夊幙丒帟悜暋崌懱傪嵞惗偟偆傞娫梩宯姴嵶朎暘棧朄偺奐敪
- 帟悜偺憂彎帯桙儊僇僯僘儉偺夝愅
- 惗暔妛揑暍悜嵻偺奐敪
- 帟壢梡僪儕儖偺夣壒壔傪傔偞偟偨尋媶
- 僆儞僨儅儞僪乽怘儕僘儉乿應掕丒昡壙僔僗僥儉偺奐敪
- 僨儞僞儖僶僀僆僼傿儖儉偺宍惉儊僇僯僘儉偺夝愅偲惂屼朄偺妋棫
- 崻柺偆怚偵偍偗傞僶僀僆僼傿儖儉嵶嬠憄偺夝柧偲梷惂朄偺妋棫
- 擄帯惈崻愲惈帟廃墛偵偍偗傞嵶嬠僶僀僆僼傿儖儉偺幚懺専嶕偲梷惂丒帯椕朄偺奐敪
- P. gingivalis 偵傛傞柶塽梷惂儊僇僯僘儉偺夝柧
検巕價乕儉媄弍PIXE/PIGE偵傛傞乽嶍傜側偄乿偆怚帯椕偺幚尰
偆怚乮傓偟帟乯偼僸僩偑嵟傕崅昿搙偵滊姵偡傞姶愼徢偱偁傝懕偗偰偍傝丄帟偺僄僫儊儖幙傗徾夊幙傪峔惉偡傞僴僀僪儘僉僔傾僷僞僀僩惉暘偑丄嵶嬠偑嶻惗偡傞巁偱梟弌偟偰恑峴偟傑偡丅偆怚偺乽扙奃乿偲乽嵞愇奃壔乿傪孞曉偡僟僀僫儈僢僋側夁掱偵偍偄偰丄帟傪峔惉偡傞Ca丄F丄Sr丄Zn丄P丄Cu側偳庬乆偺僀僆儞偺婡擻傪嵟戝尷偵敪婗偝偣傞偙偲偵傛傝丄偆怚偐傜帺屓杊屼偁傞偄偼帺屓廋暅偡傞乽僶僀僆儈僱儔儕僛乕僔儑儞乿偼棟榑揑偵偼壜擻偱偡丅偟偐偟尰忬偼丄偆怚傊偺娭梌偑帵嵈偝傟偰偄傞偦傟偧傟偺僀僆儞偺摦懺偍傛傃婡擻偺徻嵶偼枹偩偵夝柧偝傟偰偄側偄偨傔丄偆怚帯椕偼夋堦揑偵乽嶍偭偰媗傔傞乿偲偄偆媽棃偺庤朄偐傜慡偔恑揥傪尒側偄傑傑偱偡丅
丂杮尋媶偱偼丄乽嶍偭偰媗傔傞乿偲偄偆廬慜偺帟壢椪彴傪丄僶僀僆儈僱儔儕僛乕僔儑儞傪婎幉偲偟偨惗暔妛揑側偆怚梊杊丒帯椕傊偲戝偒偔曄姺偝偣傞偲偄偆棟擮偺傕偲偵丄検巕價乕儉傪墳梡偟偨尨巕丒揹巕儗儀儖偺挻惛枾峔憿丒婡擻夝愅偵傛偭偰丄偆怚偺敪徢偍傛傃恑峴梷惂偵Ca丄F丄Sr丄Zn丄P丄Cu偲偄偭偨帟幙峔惉尦慺偑擛壗側傞儊僇僯僘儉偱憈岟偟偰偄傞偐傪夝偒柧偐偡偙偲傪偹傜偭偰偄傑偡丅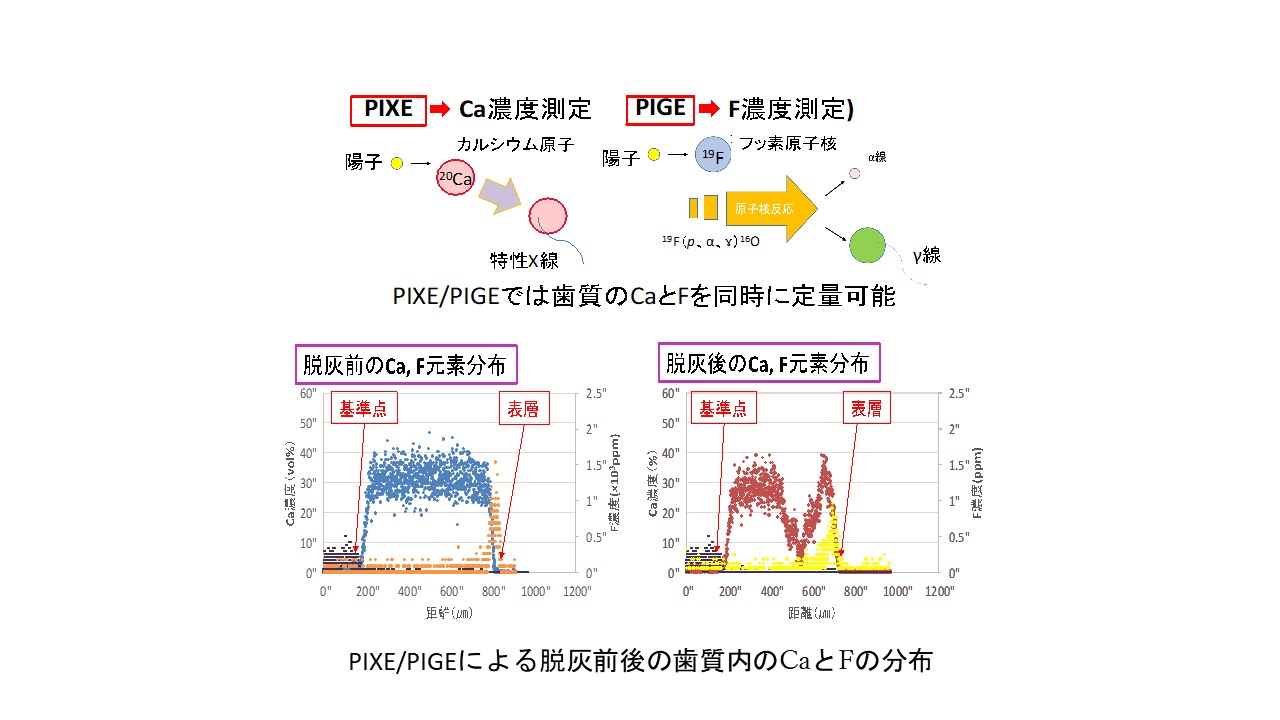
僶僀僆儈僱儔儕僛乕僔儑儞丒儊僇僯僘儉偵婎偯偔崅楊幰偺偆怚梊杊丒帯椕朄偺奐敪
丂崅楊幰偺偆怚偼憹壛偺堦搑傪偨偳偭偰偍傝丄夝寛偡傋偒媔嬞偺壽戣偲側偭偰偄傑偡丅偙傟傑偱偵丄偆怚偺昡壙朄偲偟偰摿惈 X 慄偍傛傃兞慄傪墳梡偟丄旕攋夡偵偰儈僱儔儖尦慺偺楢懕掕検丒掕惈朄傪妋棫偟偰丄奺尦慺偺偆怚恑峴梷惂偺岠壥傪専徹偟偰偒傑偟偨丅堦曽丄偆怚偺恑峴傗帟幙偺昡壙偵偼丄儈僱儔儖偺傒側傜偢僐儔乕僎儞偺惈幙偑塭嬁偟偰偄傞偙偲傕柧傜偐偵偟偰偄傑偡丅杮尋媶偱偼丄崅楊幰偺偆怚偺摿幙傪傆傑偊偰丄乽悈梟怹摟惈僇儖僔僂儉揧壛偵傛傞挻岠棪揑愇奃壔偺幚尰乿丄乽暘巕娫壦嫶宍惉偵傛傞僐儔乕僎儞偺嫮壔乿丄乽暘夝峺慺偺晄妶惈壔偵傛傞僐儔乕僎儞偺曐岇乿丄偺娤揰偐傜帟偺僶僀僆儈僱儔儕僛乕僔儑儞傪懀恑偟偰丄廬慜偺乽嶍偭偰媗傔傞乿帯椕偐傜扙媝偟丄惗暔妛揑側崅楊幰偺偆怚偺梊杊丒帯椕朄偺妋棫傪栚揑偲偟偰偄傑偡丅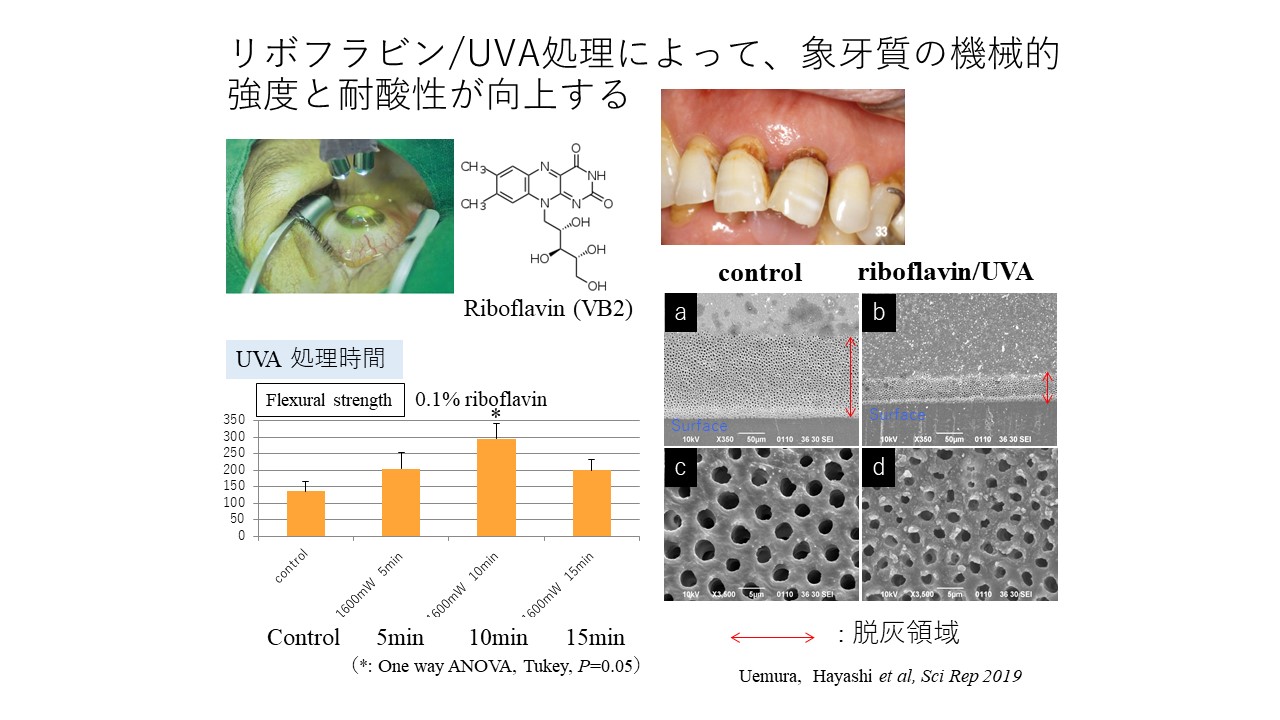
幐妶帟偺岠壥揑側曗嫮曽朄偺扵嶕
丂幐妶帟偺帟崻攋愜偼丄挿擭偵傢偨偭偰夝寛偡傋偒椪彴壽戣偱偡丅帟崻攋愜偺敪惗偵偼懡偔偺梫場偑娭梌偟偰偄傞偑丄巟戜抸憿朄傕廳梫側場巕偺堦偮偱偡丅嬤擭偼丄帟幙曐懚揑偱曗嫮岠壥偑婜懸偱偒傞巟戜抸憿朄偲偟偰丄抏惈學悢偑徾夊幙偵嬤帡偟偨僼傽僀僶乕億僗僩偲徾夊幙愙拝僔僗僥儉傪暪梡偟偨儗僕儞僐傾偑晛媦偟偰偒傑偟偨丅偟偐偟丄廋暅張抲傪孞曉偟庴恌偡傞側偳偟偰丄巆懚帟幙偑彮側偔側偭偨幐妶帟偺曗嫮偵娭偟偰偼丄廫暘偵尋媶偝傟偰偄側偄偺偑尰忬偱偡丅
丂変乆偼丄渖敄壔偟偨幐妶帟傪岠壥揑偵曗嫮偡傞偙偲傪栚揑偲偟偰丄僗儕乕僽忬丄曻幩忬丄CAD/CAM僨傿僗僋側偳條乆側宍忬偺僼傽僀僶乕嵽椏偲愙拝惈儗僕儞偺僐儞價僱乕僔儑儞偵傛偭偰攋夡掞峈惈偑嵟戝偲側傞巟戜抸憿朄傪丄惷揑丒摦揑攋夡帋尡丄偍傛傃桳尷梫慺朄夝愅傛傝扵嶕偟偰偄傑偡丅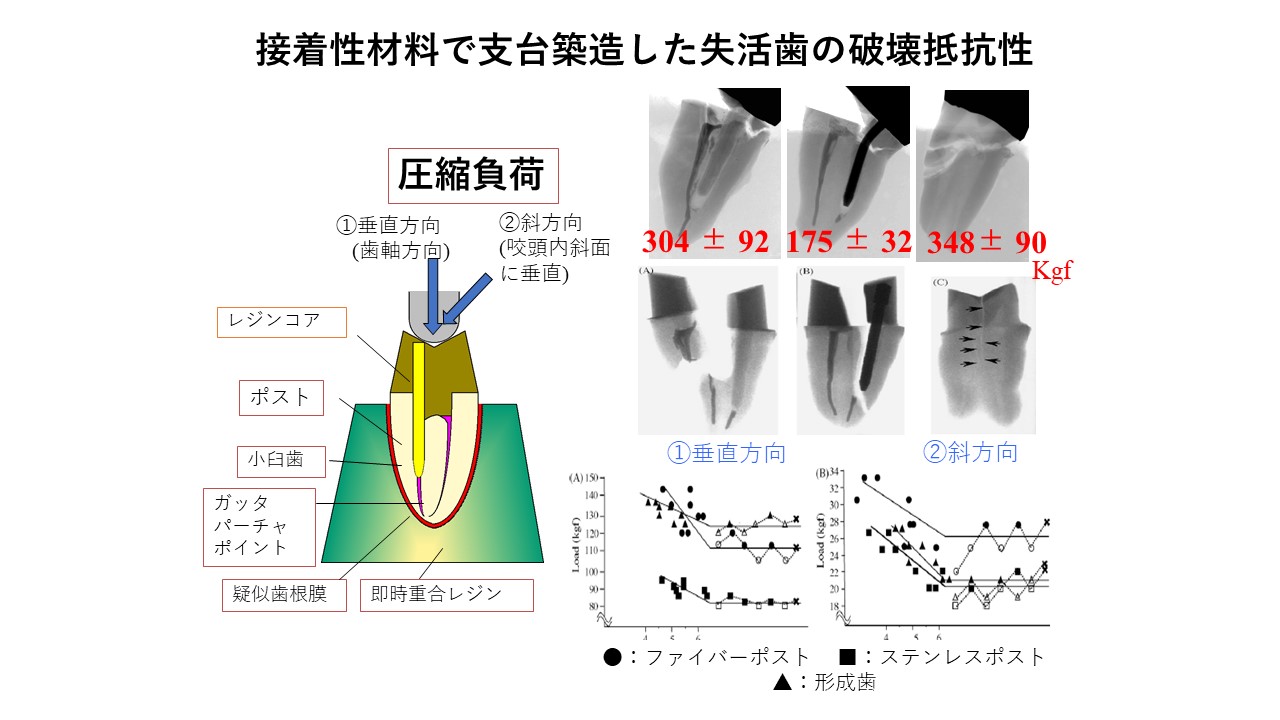
僨乕僞儅僀僯儞僌庤朄傪梡偄偨僇儕僄僗儕僗僋梊應
丂偆怚偺儅僱僕儊儞僩偵偍偄偰丄儕僗僋傾僙僗儊儞僩偼昁恵偱偁傝丄偦偺忣曬傪傕偲偵丄姵幰偦傟偧傟偵揔偟偨儊僀儞僥僫儞僗僔僗僥儉傪採埬偡傞偙偲偲側傝傑偡丅偙傟傑偱偵丄彫帣偺儕僗僋傾僙僗儊儞僩偼悢乆偺採埬偑側偝傟偰偒傑偟偨偑丄戝恖偵娭偟偰偼廫暘偵専摙偝傟偰偄傞偲偼尵偊傑偣傫丅
丂変乆偼丄掕婜揑側儊僀儞僥僫儞僗傪幚巤偟偰偄傞椪彴帟壢堛偺僨乕僞傪廂廤偟丄鑷抣傪傕偭偰儕僗僋場巕傪摿掕偡傞丄僨乕僞儅僀僯儞僌偺庤朄偵偰丄偆怚偺僴僀儕僗僋孮偲儘乕儕僗僋孮傪幆暿偡傞偙偲偵惉岟偟傑偟偨丅戝恖偺偆怚儕僗僋傾僙僗儊儞僩偱偼丄弶敪偆怚偲擇師偆怚傪暿偵暘愅偡傞偙偲偑娞梫偱偁傞偙偲偑帵偝傟傑偟偨丅傑偨暘愅寢壥偐傜丄掕婜揑側儊僀儞僥僫儞僗偵偰弶敪偆怚偼梊杊壜擻偱偁傝丄壜擻側尷傝廋暅傪峴傢偢偵偆怚儅僱僕儊儞僩傪採嫙偡傞偙偲偑丄偆怚儘乕儕僗僋偱偁傝懕偗傞尞偱偁傞偙偲偑暘偐傝傑偟偨丅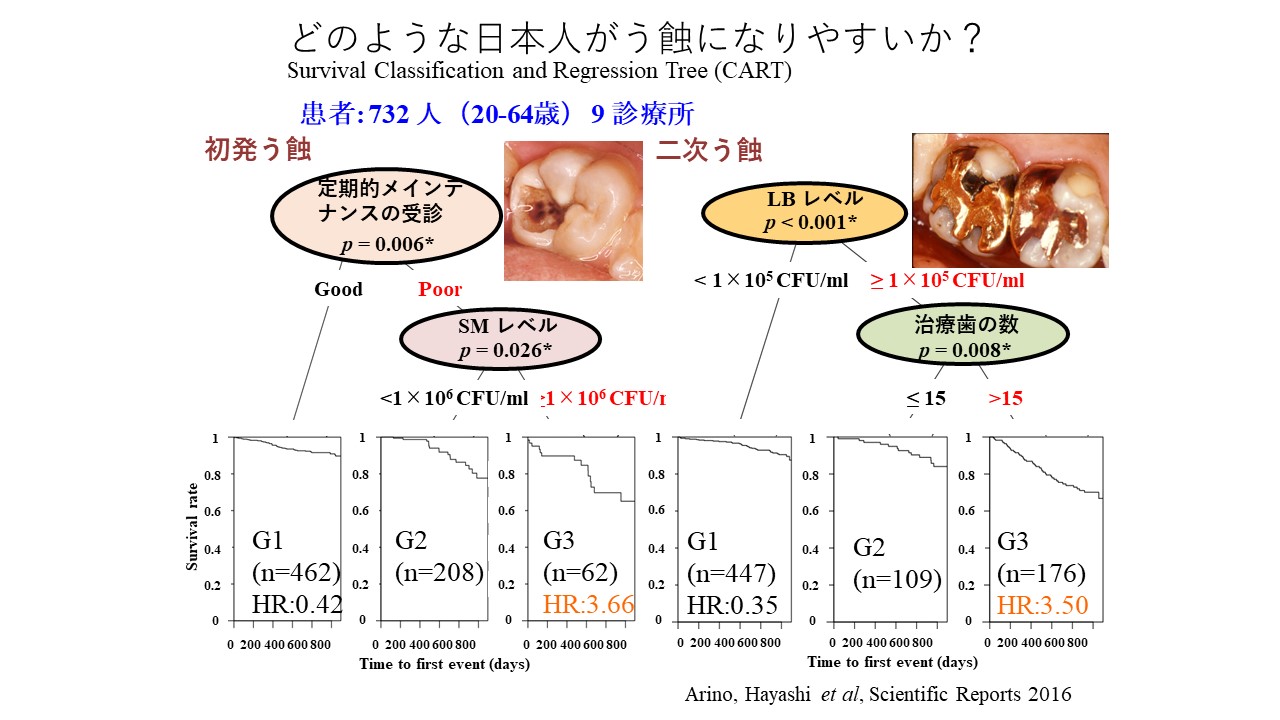
柶塽丒崪戙幱偺晩妶壔偵傛傞帯桙懀恑傪慱偭偨師悽戙崻娗揬栻嵻偺奐敪
丂擔乆偺椪彴偱椙偔憳嬾偡傞丄崻愲惈帟廃墛敪徢偺婲場偲偟偰偼丄崻娗撪偵愽傓僶僋僥儕傾偺廻庡撪傊偺怤擖偑嫇偘傜傟傑偡丅偡傞偲丄峈尨採帵嵶朎偑僶僋僥儕傾側偳偺怤擖傪俿嵶朎偵抦傜偣丄俿嵶朎偼丄僒僀僩僇僀儞傪嶻惗偟傑偡丅偙偺僒僀僩僇僀儞偼丄俛嵶朎偵摥偒丄峈懱傪嶻惗偝偣丄僶僋僥儕傾傪嬱拃偟傑偡丅堦曽偱丄俿嵶朎偵傛偭偰嶻惗偝傟偨僒僀僩僇僀儞偼丄攋崪嵶朎偵傕摥偒丄帟憛崪傪梟偐偟傑偡丅偦偺寢壥丄崻愲昦曄傪宍惉偟傑偡丅偙偺傛偆偵崻愲惈帟廃墛偼丄柶塽墳摎偲崪戙幱偺俀偮偺場巕偵傛偭偰惗偠傑偡丅偦偟偰丄偙傟傜柶塽墳摎偲崪戙幱偼丄嵶朎撪僔僌僫儖揱払宱楬偵傛偭偰惂屼偝傟偰偄傑偡丅偲偙傠偱丄尰嵼偺堦斒揑側崻娗帯椕偼丄婡夿揑側崻娗惔憒偲崻娗揬栻嵻偵傛傞崻娗撪偺柍嬠壔傪栚巜偟丄崻娗廩揢傪峴偄傑偡丅偦傟偵懳偟偰丄巹偨偪偼丄柶塽墳摎偲崪戙幱傪惂屼偡傞僔僌僫儖揱払宱楬傪晩妶壔偡傞崻娗揬栻嵻偵偰揬栻屻丄崻娗廩揢偡傞偲偄偆怴偟偄帯椕朄傪妋棫偡傞偨傔偵丄柶塽墳摎丒崪戙幱傪晩妶壔偡傞僶僀僆傾僋僥傿僽側崻娗揬栻嵻傪尰嵼丄奐敪偟偰偄傑偡丅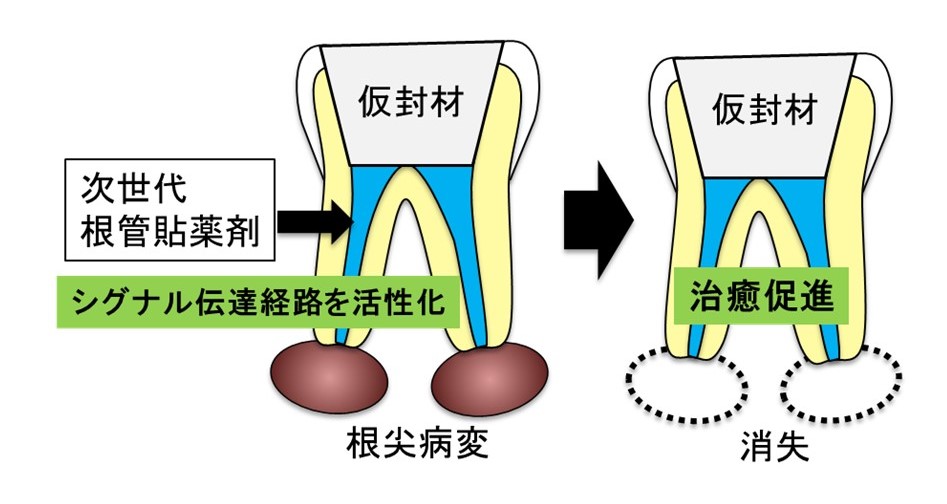
徾夊幙丒帟悜暋崌懱傪嵞惗偟偆傞娫梩宯姴嵶朎暘棧朄偺奐敪
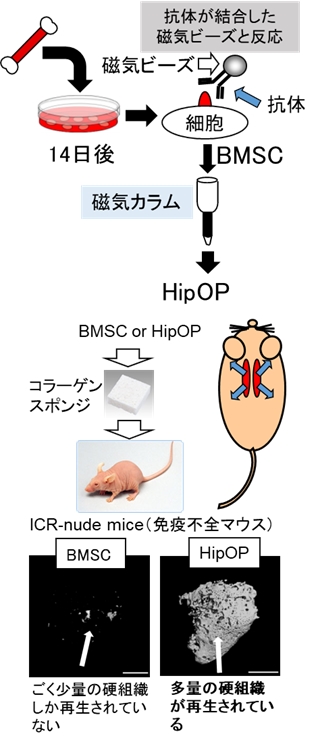
丂徾夊幙丒帟悜暋崌懱傪夞暅偡傞帯椕朄偲偟偰丄姴嵶朎偵傛傞慻怐嵞惗椕朄偑桳岠偱偁傞偲採彞偝傟偰偼偄傑偡偑丄姰慡偵偼妋棫偝傟偰偄傑偣傫丅偦偺堦偮偺梫場偲偟偰丄娫梩宯姴嵶朎偺惓懱偑敾柧偟偰偄側偄偙偲偑嫇偘傜傟傑偡丅巹偨偪偼丄娫梩宯姴嵶朎偺暘棧偵偼丄暋悢偺嵶朎昞柺儅乕僇乕傪棙梡偟偰偺壗抜奒偐偺惛惢僗僥僢僾偑昁梫偱偁傞偲峫偊傑偟偨丅偦偙偱丄戞堦抜奒偺姴嵶朎擹弅朄偺奐敪偵拝庤偟丄恾偵帵偡傛偆側怴婯姴嵶朎廤抍偺惛惢朄傪尒弌偟傑偟偨(Itoh S et al., J Cell Biochem, 2009)丅偙偺怴婯姴嵶朎傪梡偄偨嵶朎堏怉幚尡傪偍偙側偭偨偲偙傠丄擹弅慜偺嵶朎廤抍(BMSC)偵斾傋偰丄峝慻怐嵞惗擻偑100攞傕崅偄偙偲偑儅僀僋儘CT夝愅偱柧傜偐偲側傝傑偟偨丅偙偺夝愅寢壥偐傜丄偙偺怴婯姴嵶朎廤抍偼丄旕忢偵崅偄峝慻怐嵞惗擻傪傕偭偰偄傞偙偲偐傜丄曋媂揑偵 HipOP乮Highlypurified Osteo-Progenitors乯偲柦柤偟傑偟偨丅巹偨偪偼丄偙偺怴偟偔尒弌偟偨擹弅娫梩宯姴嵶朎廤抍(HipOP)傪梡偄偰丄僙儖僜乕僞乕偵傛傞姴嵶朎扨棧朄傪奐敪偟偰偄傑偡丅
帟悜偺憂彎帯桙儊僇僯僘儉偺夝愅
丂Mineral trioxide aggregate (MTA) 偼捈愙暍悜嵻偲偟偰峀偔帟壢椪彴偵庴偗擖傟傜傟偰偄傑偡偑丄峝慻怐宍惉傪摿挜偲偟偨憂彎帯桙儊僇僯僘儉偼枹偩偵柧傜偐偲側偭偰偄側偄偨傔丄棟憐揑側暍悜嵻偲偼尵偊傑偣傫丅偙偺偙偲偼捈愙暍悜嵻偺椪彴惉愌偑100亾偱偼側偄偙偲丄捈愙暍悜張抲偑堦斒椪彴壠偱幚巤傪偨傔傜傢傟傞堦場偲側偭偰偄傑偡丅変乆偼帟悜偺憂彎帯桙儊僇僯僘儉傪夝柧偟丄帯桙儊僇僯僘儉偵婎偯偄偨暍悜嵻奐敪傪揥奐偟偰偄傑偡丅鈢摯宍惉屻偺帟悜偵偍偗傞堚揱巕夝愅傪栐梾揑偵峴偭偨寢壥丄嵶朎奜儅僩儕僢僋僗偺暘夝峺慺偲偟偰拞怱揑側栶妱傪帩偮MMP暘巕偑摿堎揑側敪尰傪帵偟丄MMP暘巕偑徾夊幙偺桳婡惉暘偱偁傞徾夊幙婎幙 (Dentin matrix component, DMC)偵嶌梡偡傞偙偲偱丄帟悜偺憂彎帯桙傪懀恑偟偰偄傞偙偲傪曬崘偟傑偟偨(壓恾)丅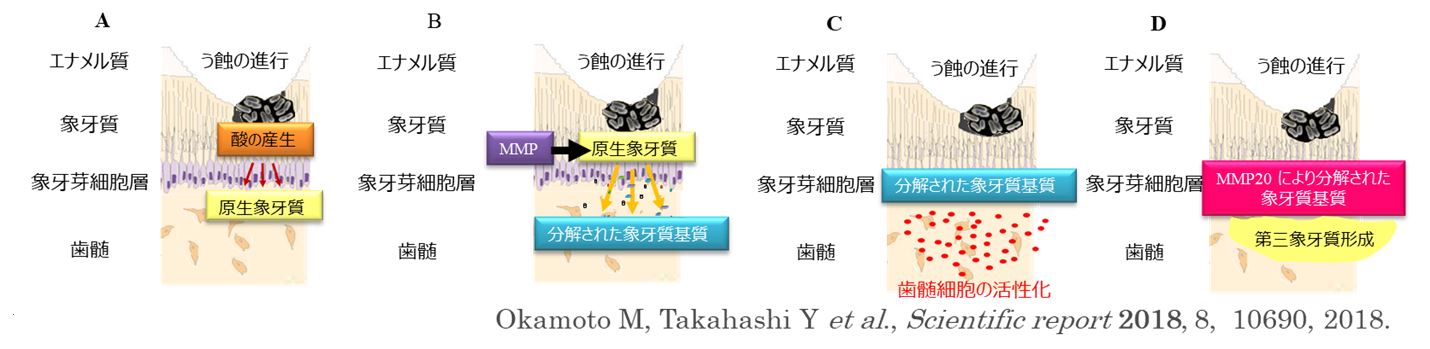
丂偝傜偵揥奐傪恑傔丄MMP偵傛傝暘夝傪庴偗偨徾夊幙婎幙拞偵娷傑傟傞帟悜憂彎帯桙懀恑場巕傪塼懱僋儘儅僩僌儔僼傿乕傪梡偄偰4偮偺岓曗場巕傑偱峣傝崬傓偙偲偵惉岟偟丄偙傟傜偺場巕偑帟悜偺憂彎帯桙傪懀恑偡傞偙偲傪尒弌偟丄奺乆偺暘巕偺帟悜慻怐偵懳偡傞塭嬁暘巕惗暔妛揑側庤朄傪墳梡偟偰徻嵶偵専摙偟偰偄傑偡(壓恾)丅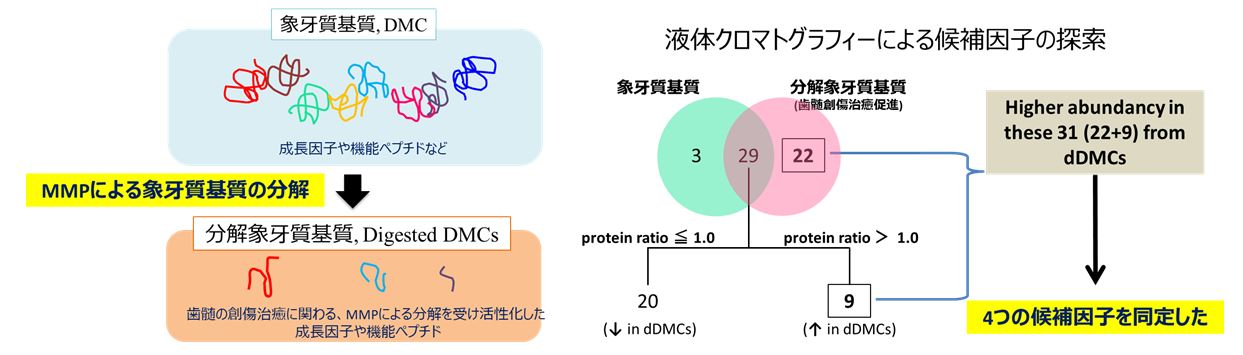
惗暔妛揑暍悜嵻偺奐敪
丂変乆偼摨掕偟偨4場巕偺棫懱峔憿夝愅偍傛傃帟悜嵶朎偺昗揑庴梕懱傪撍偒巭傔傞偙偲偱丄帟悜憂彎帯桙儊僇僯僘儉偵婎偯偄偨暍悜嵻奐敪傪恑傔傞偲偲傕偵丄暍悜嵻偲偟偰墳梡偡傞嵺偺桳岠側扴懱偺柾嶕傗幚嵺偵捈愙暍悜偑峴傢傟傞椪彴娐嫬偱偁傞丄偆怚傗帟悜墛傪恖岺揑偵敪惗偝偣偨摦暔儌僨儖傪奐敪傕恑傔偰偄傞偲偲傕偵丄婛懚嵽椏傪夵椙偡傞偙偲偱帟悜嵶朎偵梌偊傞塭嬁傪昡壙偡傞偙偲偱忋婰偲偼堎側傞懁柺偐傜帟悜偺憂彎帯桙偵敆傞尋媶傪幚巤偟偰偄傑偡丅
帟壢梡僪儕儖偺夣壒壔傪傔偞偟偨尋媶
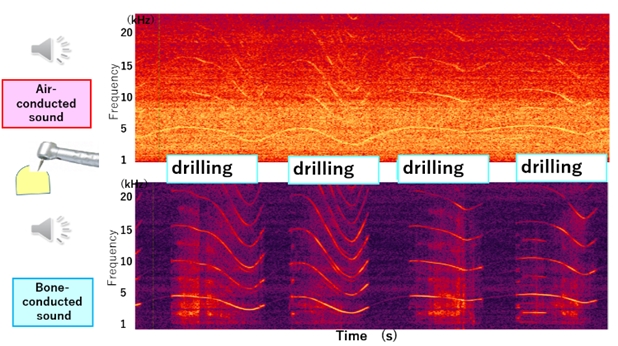
丂帟壢僪儕儖偼帟偺帯椕偵寚偐偣側偄婡婍偱偁傞堦曽偱丄敪惗偡傞壒偼擇恖偵堦恖偑晄夣偵姶偠偰偄傞偲偄傢傟偰偄傑偡丅偙偺帟壢摿桳偺壒偵懳偡傞晄夣姶偼帟壢庴椕峴摦偺慾奞場巕偲側偭偰偍傝丄帟壢偱偺夣揔側壒娐嫬偺採嫙偼廳梫側壽戣偱偡丅摉嫵幒偱偼丄乽帟偐傜揱傢傞壒怣崋乿偵拝栚偟偨姵幰偺晄夣姶寉尭傪傔偞偟偨尋媶傪偡偡傔丄帟偺愗嶍帪偵姵幰偑抦妎偡傞崪摫偍傛傃婥摫愗嶍壒偺摨帪寁應僔僗僥儉傪峔抸偟偰丄怱棟揑丄暔棟揑丄婡夿揑側専摙傪峴偭偰偄傑偡乮恾乯丅
僆儞僨儅儞僪乽怘儕僘儉乿應掕丒昡壙僔僗僥儉偺奐敪
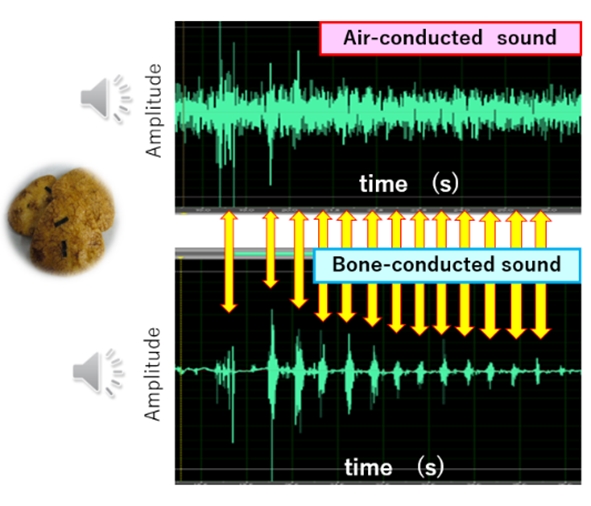
丂寬峃庻柦偺墑怢偵岦偗偰丄帟偲岥偺寬峃傪庣傝丄怘傋曽傪捠偟偨怘堢偺廳梫惈偑崅傑偭偰偄傑偡丅岤惗楯摥徣偵偍偄偰僗儘乕僈儞乽姎儈儞僌30乮30夞姎傒傑偟傚偆乯乿偑採彞偝傟偰偍傝丄枩曕寁傗実懷宆怱揹寁偺傛偆偵乽怘乿傪媞娤揑偵偲傜偊傞偙偲偑媮傔傜傟偰偄傑偡丅摉嫵幒偱偼丄怘峴摦慡懱傪乽怘儕僘儉乮怘帠拞偺欚殣夞悢丒儕僘儉丄姎傓椡丄堸怘偺昿搙傗憤帪娫乯乿偲偄偆怴偨側奣擮偱偲傜偊丄崪摫傪棙梡偟偨怘儕僘儉傪婰榐偱偒傞怴偨側應掕朄乮恾乯偍傛傃昡壙僔僗僥儉偺奐敪傪傔偞偟偰偄傑偡丅
僨儞僞儖僶僀僆僼傿儖儉偺宍惉儊僇僯僘儉偺夝愅偲惂屼朄偺妋棫
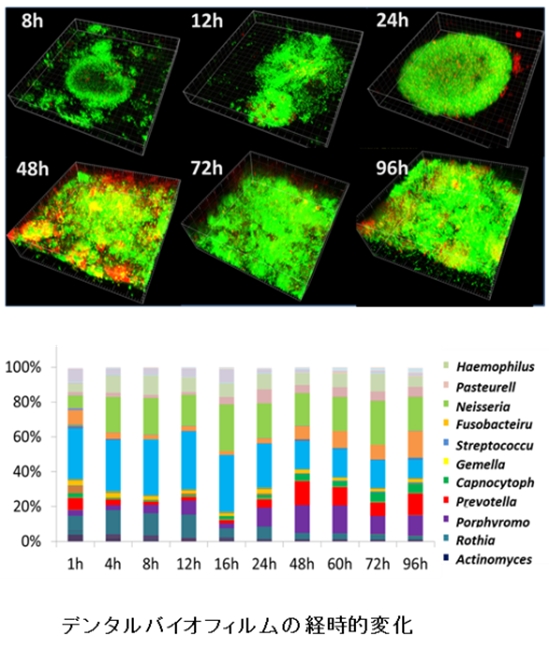
丂偆怚傗帟廃昦偲偄偭偨岥峯姶愼徢偺庡場偱偁傞僨儞僞儖僶僀僆僼傿儖儉偵偮偄偰懡柺揑側尋媶傪幚巤偟偰偄傑偡丅岠壥揑側僨儞僞儖僶僀僆僼傿儖儉惂屼朄偺妋棫傪栚巜偟丄偝傑偞傑側忦審壓偵偍偗傞僨儞僞儖僶僀僆僼傿儖儉宍惉偺幚懺傪慻怐丒宍懺妛揑偵専嶕偡傞偲偲傕偵丄暘巕惗暔妛揑庤朄偵傛傝懡柺揑偵夝愅偟偰偄傑偡丅
Wake N, Asahi Y, Noiri Y, Hayashi M, Motooka D, Nakamura S, Gotoh K, Miura J, Machi H, Iida T, Ebisu S, Temporal dynamics of bacterial microbiota in the human oral cavity determined using an in situ model of dental biofilms, npj Biofilms and Microbiome, 2:16018, 2016.
崻柺偆怚偵偍偗傞僶僀僆僼傿儖儉嵶嬠憄偺夝柧偲梷惂朄偺妋棫
丂崻柺偆怚昦曄傛傝嵦庢偟偨椪彴僒儞僾儖傪夝愅偡傞偙偲偱丄崻柺偆怚偵娭楢偡傞嵶嬠憄傪夝柧偟傑偡丅偝傜偵丄崻柺偆怚傪柾曧偟偨in situ僶僀僆僼傿儖儉儌僨儖傪妋棫偟丄崻柺偆怚偵岠壥揑側梷惂朄傪専摙偟傑偡丅
擄帯惈崻愲惈帟廃墛偵偍偗傞嵶嬠僶僀僆僼傿儖儉偺幚懺専嶕偲梷惂丒帯椕朄偺奐敪
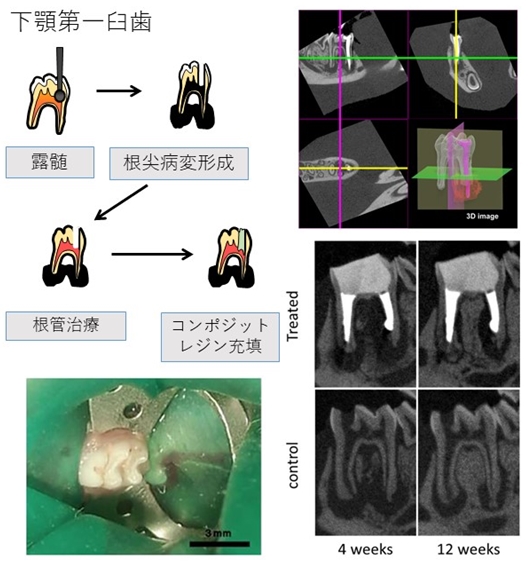
丂捠忢偺崻娗帯椕傪峴偭偰傕帯桙偟側偄擄帯惈崻愲惈帟廃墛偺尨場偺傂偲偮偲偟偰丄崻愲岴奜偵宍惉偝傟偨僶僀僆僼傿儖儉偑娭楢偡傞偲偄偆曬崘偑偁傝傑偡丅偦偙偱丄in vivo偵偰崻愲岴奜僶僀僆僼傿儖儉傪幚尡揑偵宍惉偝偣丄擄帯惈崻愲惈帟廃墛偺敪徢婡彉偵偮偄偰専嶕偟傑偡丅傑偨丄幚尡揑偵嶌惢偟偨崻愲昦曄偵懳偟丄怴婯栻嵻側偳傪揔梡偟丄擄帯惈崻愲惈帟廃墛偵懳偡傞怴婯梷惂朄丒帯椕朄偵偮側偑傞尋媶傪峴偭偰偄傑偡丅
Yoneda N, Noiri Y, Matsui S, Kuremoto K, Maezono H, Ishimoto T, Nakano T, Ebisu S, Hayashi M. Development of a root canal treatment model in the rat. Sci Rep. 12; 7: 3315, 2017.
Kuremoto K, Noiri Y, Ishimoto T, Yoneda N, Yamamoto R, Maezono H, Nakano T, Hayashi M, Ebisu S. Promotion of endodontic lesions in rats by a novel extraradicular biofilm model using obturation materials. Appl Environ Microbiol. 80: 3804-10, 2014.
P. gingivalis 偵傛傞柶塽梷惂儊僇僯僘儉偺夝柧
丂Porphyromonas gingivalis偼丄曈墢惈偍傛傃崻愲惈帟廃墛偺枬惈壔偵娭傢傞庡梫側昦尨惈嵶嬠偲偟偰拲栚偝傟偰偄傑偡丅傑偨嬤擭偱偼丄偙傟傑偱嵶朎奜偱偺傒憹怋偡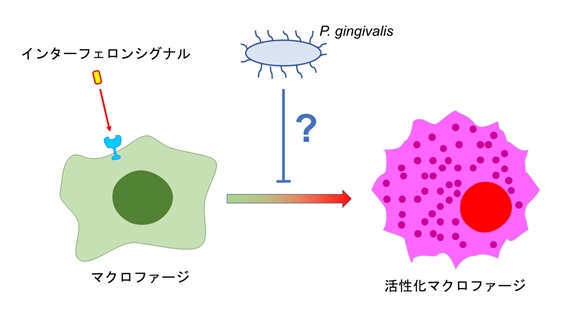 傞偲峫偊傜傟偰偄偨P.gingivalis偑嵶朎撪偵怤擖偡傞偙偲偱廻庡偺柶塽宯傪夞旔偟丄昦懺傪恑峴丒慗墑壔偝偣偰偄傞壜擻惈偑帵嵈偝傟偰偍傝丄偦偺嵶朎撪偵偍偗傞摦懺偺夝柧偑媫柋偲側偭偰偒偰偄傑偡丅
傞偲峫偊傜傟偰偄偨P.gingivalis偑嵶朎撪偵怤擖偡傞偙偲偱廻庡偺柶塽宯傪夞旔偟丄昦懺傪恑峴丒慗墑壔偝偣偰偄傞壜擻惈偑帵嵈偝傟偰偍傝丄偦偺嵶朎撪偵偍偗傞摦懺偺夝柧偑媫柋偲側偭偰偒偰偄傑偡丅
嵶朎撪偵怤擖偟偨昦尨懱偵懳偡傞廻庡懁偺姶愼杊屼偵偼丄僀儞僞乕僼僃儘儞偵傛偭偰桿摫偝傟傞柶塽婡峔偑偒傢傔偰廳梫偱偁傞偙偲偑抦傜傟偰偄傑偡丅椺偊偽僀儞僞乕僼僃儘儞偺堦庬偱偁傞IFN-兞乮僀儞僞乕僼僃儘儞-僈儞儅乯偼儅僋儘僼傽乕僕傪妶惈壔偟偰栺2,000庬椶偺堚揱巕敪尰傪桿摫偟丄偙傟傜偺桿摫偝傟偨暘巕孮偑嵶朎撪偺昦尨懱攔彍偵廳梫側摥偒傪偟傑偡丅
丂巹偨偪偑峴偭偨梊旛幚尡偺寢壥偐傜丄P. gingivalis偑帟擏忋旂嵶朎偵偍偄偰條乆側僀儞僞乕僼僃儘儞僔僌僫儖娭楢堚揱巕偺敪尰傪梷惂偡傞偙偲偑柧傜偐偵側傝傑偟偨乮恾乯丅
丂偙傟傜傪攚宨偵杮尋媶偱偼丄乽P. gingivalis 偑偄偐偵偟偰僀儞僞乕僼僃儘儞僔僌僫儖偺梷惂偡傞偺偐乿丄偦偟偰乽P. gingivalis 偵傛傞廻庡柶塽偺梷惂偑嬶懱揑偵偳偺傛偆偵幘姵偺恑揥傗慗墑惈偵婑梌偡傞偺偐乿偲偄偆栤偄傪媶柧偡傞偙偲偱丄P. gingivalis 偵傛傞帟廃幘姵偺昦懺宍惉傪懀恑偝偣傞怴婯儊僇僯僘儉偺夝柧傪栚巜偟偰偄傑偡丅